Enzymen
definitie
Enzymen zijn chemische stoffen die overal in het lichaam voorkomen. Ze zetten chemische reacties in beweging in het lichaam.
geschiedenis
Het woord enzym was van Wilhelm Friedrich Kühne 1878 en is afgeleid van het Griekse woord enzymon, wat gist of zuurdesem betekent. Dit vond vervolgens zijn weg naar de internationale wetenschap. De internationale unie van pure toegepaste chemie (IUPAC) en de internationale unie van biochemie (IUBMB) werkten een nomenclatuur uit voor de enzymen, die de vertegenwoordigers van deze grote groep stoffen als een gemeenschappelijke groep definieert. De naamgeving, die de enzymen naar hun taken classificeert, is belangrijk voor het bepalen van de taken van de individuele enzymen.
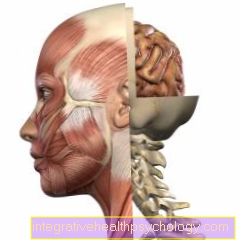
Illustratie van enzymen
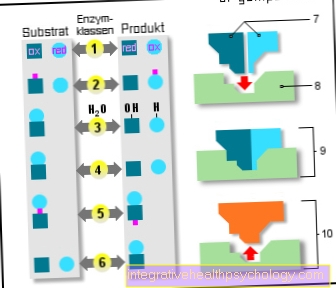
Enzymen
6 enzymklassen:
- Oxidoreductases
(Oxidatie / reductie) - Transferases
(Overdragen) - Hydrolasen
(Gebruik van water) - Lyases
(Decollete) - Isomerasen
(dezelfde moleculaire formule) - Ligasen
(Toevoegingsreacties) - Substraten
- Actief centrum
- Enzym / substraat
complex - Enzym / product
complex
Een overzicht van allemaalDe afbeeldingen van Dr-Gumpert zijn te vinden op: medische illustraties
Benoemen
De Benoemen het enzym is aan drie basisprincipes gebaseerd.Enzymnamen die eindigen op -ase beschrijven verschillende enzymen in een systeem. De enzymnaam zelf beschrijft de reactie die het enzym in gang zet (gekatalyseerd). De enzymnaam is ook een classificatie van het enzym. Daarnaast een codesysteem dat EG-nummersysteem, waarin de enzymen worden gemaakt onder een numerieke code vier cijfers is te vinden. Het eerste cijfer geeft de enzymklasse aan. Lijsten met alle gedetecteerde enzymen zorgen ervoor dat de opgegeven enzymcode sneller kan worden gevonden. Hoewel de codes zijn gebaseerd op de eigenschappen van de reactie die het enzym katalyseert, blijken numerieke codes in de praktijk onpraktisch te zijn. Systematische namen op basis van de bovenstaande regels worden vaker gebruikt. Problemen met de nomenclatuur ontstaan bijvoorbeeld bij enzymen die meerdere reacties katalyseren. Daarom zijn er soms meerdere namen voor. Sommige enzymen hebben triviale namen die niet aangeven dat de genoemde stof een enzym is. Omdat de namen traditioneel veel werden gebruikt, bleven sommige ervan behouden.
Indeling volgens enzymfunctie
Volgens IUPAC en IUBMB worden enzymen onderverdeeld in zes enzymklassen op basis van de reactie die ze initiëren:
- Oxidoreductases
Oxidoreductases zetten redoxreacties in gang. Bij deze chemische reactie gaan elektronen van de ene reactiepartner naar de andere. Er is een afgifte van elektronen (oxidatie) van de ene stof en een opname van elektronen (reductie) door een andere stof.
De formule voor de gekatalyseerde reactie is A ?? + B? A? + B?.
Stof A geeft een elektron (?) Af en wordt geoxideerd, terwijl stof B dit elektron opneemt en wordt gereduceerd. Daarom worden redoxreacties ook wel reductie-oxidatiereacties genoemd.
Veel metabolische reacties zijn redoxreacties. Oxygenases dragen een of meer zuurstofatomen over naar hun substraat. - Transferases
Transferases dragen de functionele groep over van het ene substraat naar het andere. Functionele groepen zijn atoomgroepen in organische verbindingen die in hoge mate de stofeigenschappen en het reactiegedrag bepalen. Chemische verbindingen met dezelfde functionele groepen worden vanwege hun vergelijkbare eigenschappen gegroepeerd in stofklassen. Functionele groepen worden onderverdeeld naargelang ze heteroatomen zijn of niet. Heteroatomen zijn allemaal atomen in organische verbindingen die noch koolstof, noch waterstof zijn.
Bijv.: -OH -> hydroxylgroep (alcoholen) - Hydrolasen
Hydrolasen splitsen de bindingen in omkeerbare reacties met water. Esters, esters, peptiden, glycosiden, zuuranhydriden of C-C-bindingen. De evenwichtsreactie is: A-B + H2O? A-H + B-OH.
Een enzym dat tot de groep van hydrolasen behoort, is b.v. Alfa galactosidase. - Lyases
Lyases, ook wel synthases genoemd, katalyseren de splitsing van complexe producten van eenvoudige substraten zonder ATP af te splitsen. Het reactieschema is A-B → A + B.
ATP is adenosinetrifosfaat en een nucleotide, bestaande uit het trifosfaat van het nucleoside adenosine (en daarmee een energierijke bouwsteen van het nucleïnezuur-RNA). ATP is echter vooral de universele vorm van direct beschikbare energie in elke cel en tegelijkertijd een belangrijke regulator van energieleverende processen. Indien nodig wordt ATP opnieuw gesynthetiseerd uit andere energiereserves (creatinefosfaat, glycogeen, vetzuren). Het ATP-molecuul bestaat uit een adenineresidu, de suikerribose en drie fosfaten (? To?) In ester (?) Of anhydridebindingen (? En?). - Isomerasen
Isomerasen versnellen de chemische omzetting van isomeren. Isomerie is het voorkomen van twee of meer chemische verbindingen met exact dezelfde atomen (dezelfde empirische formule) en molecuulgewichten, maar die verschillen in de verbinding of de ruimtelijke ordening van de atomen. De overeenkomstige verbindingen worden isomeren genoemd.
Deze isomeren verschillen in hun chemische en / of fysische eigenschappen, en vaak ook in hun biochemische eigenschappen. Isomerie komt voornamelijk voor bij organische verbindingen, maar ook bij (anorganische) coördinatieverbindingen. De isomerie is onderverdeeld in verschillende gebieden. - Ligasen
Ligasen katalyseren de vorming van stoffen die chemisch complexer zijn dan de gebruikte substraten, maar, in tegenstelling tot de lyases, alleen enzymatisch effectief zijn bij ATP-splitsing. De vorming van deze stoffen vereist dus energie die wordt verkregen door de splitsing van ATP.
Sommige enzymen kunnen verschillende, soms heel verschillende, reacties katalyseren. Als dit het geval is, worden ze ingedeeld in verschillende enzymklassen.
Mogelijk bent u ook geïnteresseerd in deze artikelen:
- Alfa-glucosidase
- Lipase
- Trypsine
Indeling volgens enzymstructuur
Bijna alle enzymen zijn eiwitten en kunnen worden geclassificeerd op basis van de lengte van de eiwitketen:
- Monomeren
Enzymen die uit slechts één eiwitketen bestaan - Oligomeren
Enzymen die bestaan uit verschillende eiwitketens (monomeren) - Multi-enzymketens
Verschillende geaggregeerde enzymen die samenwerken en elkaar reguleren. Deze enzymketens katalyseren de opeenvolgende stappen in het metabolisme van de cel.
Daarnaast zijn er individuele eiwitketens die meerdere enzymactiviteiten bevatten; dit worden multifunctionele enzymen genoemd.
Indeling volgens cofactoren
Een andere classificatie is de classificatie volgens de overweging van de cofactoren. Cofactoren, co-enzymen en co-substraten zijn namen voor verschillende classificaties van stoffen die biochemische reacties beïnvloeden door hun interactie met enzymen.
Er wordt rekening gehouden met organische moleculen en ionen (meestal metaalionen).
De zuivere proteïne-enzymen bestaan uitsluitend uit proteïnen en het actieve centrum wordt enkel gevormd uit aminozuurresten en de peptideskelet. Aminozuren zijn een klasse organische verbindingen met ten minste één carboxygroep (-COOH) en één aminogroep (-NH2).
De holo-enzymen bestaan uit een eiwitcomponent, het apoenzym en een cofactor, een molecuul met een laag molecuulgewicht (geen eiwit). Beiden samen zijn belangrijk voor de functie van het enzym.
Co-enzymen
Organische moleculen als cofactoren worden co-enzymen genoemd. Als ze covalent aan het apoenzym zijn gebonden, worden ze prothetische groepen of co-substraten genoemd. Een prothetische groep is de term die wordt gebruikt om niet-eiwitcomponenten te beschrijven die stevig (meestal covalent) zijn gebonden aan een eiwit met een katalytisch effect.
Cosubstrates zijn namen voor verschillende classificaties van stoffen die biochemische reacties beïnvloeden door hun interactie met enzymen. Als biokatalysatoren versnellen moleculen reacties in organismen, enzymen versnellen biochemische reacties. Ze verminderen de activeringsenergie die moet worden overwonnen zodat de stof kan worden omgezet.














.jpg)